이온 결합 화합물은 정전기력에 의해 서로 반대되는 전하를 가진 이온들이 이온 결합을 통해 순차적인 배열로 구성된 화합물을 말합니다. 이러한 성질을 갖는 이온결합화합물에 대한 실험식 작성 방법에 대해 설명드리겠습니다.
목차
1. 이온결합 화합물의 실험식(화학식) 표기 방법
2. 이온 전하를 이용한 이온결합 화합물 실험식 작성 방법
3. 이온결합 화합물은 실험식으로 완성
1. 이온결합 화합물의 실험식(화학식) 표기 방법
① 이온으로 이루어진 물질은 성분 원소의 원소 기호와 이온의 결합 개수비로 표현할 수 있습니다. 즉, 양이온 + 음이온의 원소 기호를 쓰고, 개수비를 구해 원소 기호의 오른쪽 아래에 작은 숫자로 표시합니다.
예)
=
② 양이온을 먼저쓰고, 다음으로 음이온을 쓴다
예)
③ 이온결합 화합물
- 전기적으로 중성이다. (개수비는 가장 작은 정수비로 한다.)
㉠ 양전하 + 음전하 = 0
㉡ (양이온의 개수 × 양이온의 전하) + (음이온의 개수 × 음이온의 전하) = 0
2. 이온 전하를 이용한 이온결합 화합물 실험식 작성 방법
① 전기적으로 중성이다
② 양전하 + 음전하 = 0이다


예)
- (+3) + (-2) ≠ 0
- 2 × (+3) + 3 × (-2) = 0
- (+2) + (-3) ≠ 0
- 3 × (+2) + 2 × (-3) = 0
- (+3) + (-1) ≠ 0
- 1 × (+3) + 3 × (-1) = 0
- (+3) + (-2) ≠ 0
- 2 × (+3) + 3 × (-2) = 0
- (+2) + (-3) ≠ 0
- 3 × (+2) + 2 × (-3) = 0
- (+2) + (-1) ≠ 0
- 1 × (+2) + 2 × (-1) = 0
- (+2) + (-3) ≠ 0
- 3 × (+2) + 2 × (-3) = 0
- (+2) + (-3) ≠ 0
- 3 × (+2) + 2 × (-3) = 0
- (+1) + (-2) ≠ 0
- 2 × (+1) + 1 × (-2) = 0
3. 이온결합 화합물은 실험식으로 완성된다
① 실험식
분자를 구성하는 원자의 종류를 상대적인 수 즉, 가장 작은 정수비로 나타낸 화학실을 말합니다.
② 아래 그림에서 정답은 1번 일까요 2번 일까요?
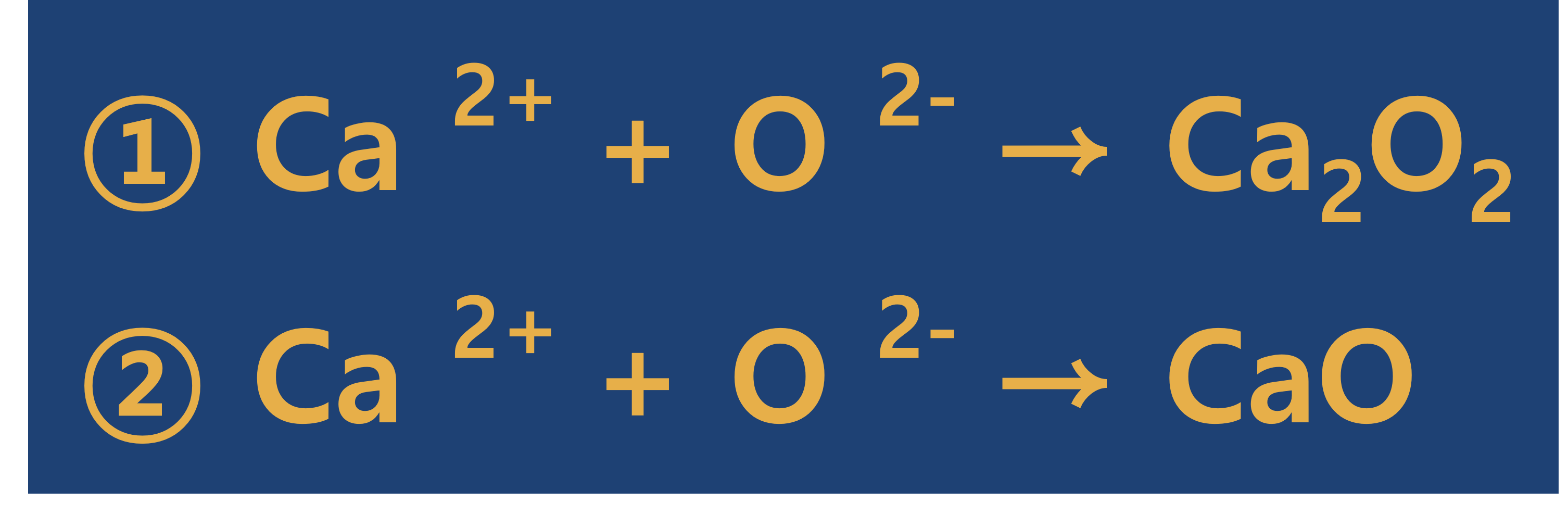
- 정답 먼저 공개하겠습니다. 정답은 2번 입니다.
이 부분에서 어려움을 느끼는 분이 계실 것 같아 추가 보충 설명 드리겠습니다.
이런 내용을 간과하고 단순하게 상대편 이온전하끼리 크로스하면 되는 것으로 알고 있으면
이번 시간에는 이온결합화합물의 실험식(화학식) 작성 방법에 대해 알아보았습니다. 조금만 신경쓰면 그렇게 어렵지 않은 내용입니다. 반드시 숙지하시어 좋은 결과와 함께 하시길 바랍니다.

'위험물 기능장 > 일반화학' 카테고리의 다른 글
| 산화-환원(redox, 酸化還元), 전자의 이동, 산화수와 산화상태 (0) | 2023.11.29 |
|---|---|
| 전기음성도(전기력), 금속의 이온화 경향, 금속과 비금속의 양쪽성 원소, 암기법 (1) | 2023.11.28 |
| 이온(양이온과 음이온), 이온결합 화합물 명명법(양이온, 음이온), 다원자 이온식 및 원자가 (0) | 2023.11.26 |
| Hill system! 화학식 표기방법(실험식, 분자식) (0) | 2023.11.26 |
| 일반화학 원소 주기율표 암기하지 말고 이해하자, 원소주기율표 만들기 치트키와 암기법 (위험물기능장 자격증 취득 대비) (0) | 2022.02.28 |




댓글